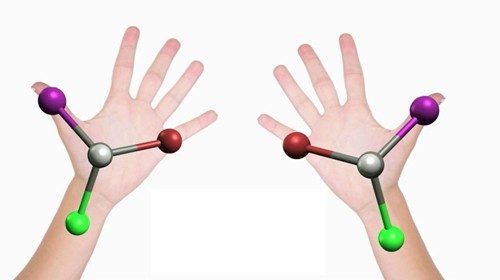
Durante il periodo di confinamento sociale, molti hanno cercato di tagliarsi i capelli allo specchio da soli. Spesso i risultati non sono stati all’altezza delle aspettative e la causa primaria di questo risultato deludente ha poco a che vedere con la mancanza di perizia nel maneggiare le forbici, quanto con un effetto innato della specularità. Quando muoviamo la mano destra verso la sinistra infatti, la nostra immagine sullo specchio sembra muovere la sua mano sinistra verso la sua destra. Questa percezione non si deve a una vera inversione del movimento, ma piuttosto al fatto che l’immagine nello specchio è esattamente uguale a quella proiettata ad eccetto di un solo asse invertito. Questo fenomeno si chiama chiralità (il nome fu coniato dal famoso fisico Lord Kelvin) poiché per capirlo basta cercare di sovrapporre la mano destra e la mano sinistra (chiralità deriva dalla parola greca “mano”), e notare che non possono essere sovrapposte per rotazione o per trasposizione quando riposte su piani orizzontali (i pollici rimangono ai lati opposti e gli indici si sovrappongono ai mignoli e i medi agli anulari).
Anche le molecole possono essere chirali. Due molecole chirali hanno la stessa composizioni di atomi nello stesso ordine, ma hanno uno atomo (o un gruppo di atomi) che è disposto o verso la destra (denominati, r - o d -) o verso la sinistra (denominati, l -) in modo che la configurazione geometrica dell’una sull’altra non risulta sovrapponibile. Questa proprietà è molto comune negli zuccheri e negli aminoacidi e per questo ha una notevole valenza biochimica. Infatti, le proteine che sono un assemblaggio di ammino-acidi, con piccole eccezioni, usano solo amminoacidi di tipo l -, e alcuni polimeri degli zuccheri (l’amido per esempio), sono biodegradabili dal nostro sistema digestivo solo se sono di uno dei due tipi.
A volte, ci sembra di conoscere le cose perché ne conosciamo la composizione (la formula chimica per esempio del glucosio fatta di 6 atomi di carbonio, sei di ossigeno e 12 di idrogeno, c6h12o6 ). Poi ci rendiamo conto che è necessario conoscere l’ordine della composizione (anche il fruttosio ha la stessa formula chimica del glucosio ma un ordine diverso; nel caso del glucosio, gli atomi del carbonio sono tutti legati in serie, nel caso del fruttosio, la serie è interrotta da un atomo di ossigeno). E alla fine, notiamo che anche la posizione geometrica conta. Tanto è vero che il metabolismo terrestre usa solo il d-glucosio (le piante producono solo d-glucosio nella fotosintesi e noi bruciamo solo il d-glucosio per produrre energia nel ciclo di Krebs). La morale è: non basta sapere di cosa sono fatte le cose, e non basta neppure sapere l’ordine degli elementi che le compongono, bisogna anche sapere la forma esatta che hanno… e anche quando sappiamo la forma, non capiamo perché la natura abbia scelto l’una e non l’altra forma visto che sono apparentemente la stessa cosa, ma allo specchio.
di Carlo Maria Polvani